Alors que la société lilloise Genfit rencontrera vendredi les analystes et les investisseurs lors du 50e congrès annuel de l’EASL (European Association for the Study of the Liver), l’américain Intercept Pharmaceuticals a annoncé ce lundi qu’il présenterait au congrès, dont il est l’un des sponsors, plusieurs abstracts évaluant l’acide obéticholique (OCA) chez des patients atteints de cirrhose biliaire primitive (CBP) et de stéatohépatite non-alcoolique (NASH).
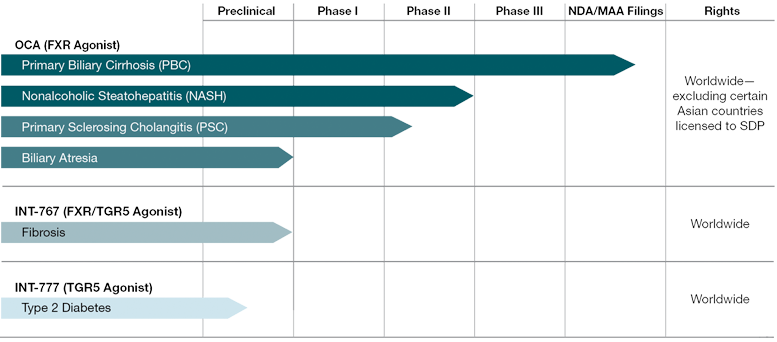
L’OCA est un agoniste du récepteur Farnesoid X (FXR) en cours de développement clinique pour un éventail de troubles chroniques du foie. Intercept a débuté le processus en vue d’obtenir de la FDA l’autorisation de mise sur le marché dans la cirrhose biliaire primitive, affection particulièrement grave (maladie de Hanot) ; la demande proprement dite devrait être déposée au deuxième trimestre 2015. L’OCA a également reçu la désignation de « Breakthrough Therapy » (le statut le plus sélectif) pour le traitement de la NASH avec fibrose hépatique.
« Nous sommes impatients de présenter les résultats relatifs à l’OCA, dans le contexte à la fois de la CBP, et de la NASH », a indiqué Mark Pruzanski, le PDG d’Intercept. « En conjonction avec les autres analyses du groupe d’étude de la CBP présentées au congrès, nous espérons présenter des résultats qui fourniront de nouvelles perspectives dans la gestion de cette maladie débilitante chronique ».
De son côté, la direction de Genfit présentera des résultats additionnels de l’étude de Phase 2b GOLDEN-505 sur son composé GFT-505, et le Pr. Philippe Lehert détaillera le plan d’analyses statistiques utilisé lors de l’étude.
L’action Intercept enregistrait un gain de 3,41 % lundi en cours de séance au Nasdaq, à 284,31 dollars, tandis que l’action Genfit a clôturé en hausse de 7,75 % à 46,25 euros. Le titre Genfit coté sur le marché de gré à gré américain poursuivait sa progression également.